Vídeo resumen
Introducción

La hipotermia accidental es la caída involuntaria de la temperatura central por debajo de 35 °C. La hipotermia accidental puede ser causada en un sujeto sano por la exposición a un ambiente frío (hipotermia accidental primaria) o desencadenada por otras condiciones, más comúnmente enfermedad, intoxicación o trauma, llamada hipotermia secundaria ( Tabla 1 ).
La fisiopatología de la hipotermia accidental en pacientes lesionados o enfermos se ha descrito en detalle en otra parte. Este artículo no cubre la hipotermia terapéutica, que es la hipotermia inducida intencionalmente utilizada en campos como la cirugía cardíaca y como parte de un paquete de cuidados posteriores a la reanimación después de un paro cardíaco en neonatos y adultos.
| Termorregulación deteriorada | Disminución de la producción de calor | Aumento de la pérdida de calor |
|---|---|---|
| Insuficiencia del sistema nervioso central | Insuficiencia endocrina | Enfermedad dermatológica |
| Anorexia nerviosa | Cetoacidosis alcohólica o diabética | Quemaduras |
| Ataque | Hipoadrenalismo | vasodilatación inducida |
| Lesión cerebral traumática | Hipopituitarismo | Medicamentos y toxinas |
| disfunción hipotalámica | Acidosis láctica | |
| Insuficiencia metabólica | Iatrogénico | |
| Neoplasma | combustible insuficiente | Parto de emergencia (posiblemente sin prevención de hipotermia) |
| enfermedad de Parkinson | Esfuerzo físico extremo | Infusiones frías |
| Efectos farmacológicos (fármacos anestésicos) | Hipoglucemia | Tratamiento del golpe de calor |
| Accidente cerebrovascular, hemorrágico o isquémico | Desnutrición | |
| Toxinas | Otros estados clínicos asociados | |
| Compromiso neuromuscular | Carcinomatosis | |
| Fallo periférico | Extremos de edad | Enfermedades cardiopulmonares |
| Transección aguda de la médula espinal | Escalofríos alterados | Infecciones importantes |
| Neuropatía periférica | Inactividad | Traumatismo múltiple |
| Choque |
A medida que se desarrolla la hipotermia accidental, las constantes vitales disminuyen hasta que se produce un paro cardíaco. La hipotermia tiene efectos perjudiciales en la función de múltiples órganos, como el corazón, el cerebro, los riñones, la coagulación sanguínea y, posiblemente, el sistema inmunitario.
En general, la hipotermia accidental aumenta la morbilidad y la mortalidad en las víctimas afectadas. El objetivo de este trabajo es proporcionar una visión general actualizada de los aspectos clínicos de la hipotermia accidental.
Epidemiología
La hipotermia accidental se reconoce desde la antigüedad. A lo largo de la historia, la hipotermia ha sido una enfermedad de guerra y desastres como avalanchas, terremotos y tsunamis. Actualmente, en los países desarrollados, la hipotermia primaria afecta principalmente a las personas que viven, trabajan y se recrean al aire libre, poniéndose en riesgo en ambientes fríos, y a las personas sin hogar.
En los países menos desarrollados, la hipotermia primaria afecta a las personas sin hogar y a las personas en accidentes masivos; por ejemplo, víctimas de avalanchas que sepultan pueblos y viajeros en áreas montañosas mal protegidas. En general, el riesgo de hipotermia accidental por exposición al frío aumenta con la disminución de la temperatura, pero muchos casos entre personas sin hogar ocurren durante períodos de estrés por frío bajo y moderado.
La hipotermia secundaria se ha reconocido como un fenómeno en ancianos y pacientes con múltiples comorbilidades, principalmente en Japón, que tiene la población más anciana del mundo.
Los países con poblaciones comparativamente mayores pueden ver aumentos similares en las próximas décadas. En Estados Unidos, la hipotermia primaria es la causa de al menos 1500 muertes al año. De 1995 a 2004, alrededor de 15 000 pacientes se presentaron anualmente a hospitales con hipotermia y otras afecciones relacionadas con el frío.
La incidencia de hipotermia accidental en países europeos y Nueva Zelanda varía de 0,13 a 6,9 casos por 100 000 por año. La hipotermia es responsable de alrededor de 2 muertes por 100 000 por año en Escocia y 5 por 100 000 por año en Polonia.
Las frecuencias varían ampliamente porque para la mayoría de los países no hay datos nacionales confiables disponibles. No hay datos epidemiológicos disponibles de países menos desarrollados en África, Sudamérica y el Sudeste Asiático.
Fisiopatología
Los seres humanos son homeotermos. La temperatura central está estrechamente regulada, con mínimas variaciones diurnas de aproximadamente 37 ± 0,5 °C. La termorregulación central (hipotalámica) y periférica (vasoconstricción y dilatación periférica, escalofríos y sudoración) regulan la temperatura central de forma autónoma ( Figura 1 ).
Los seres humanos pueden influir conscientemente en la temperatura central mediante el comportamiento, el ejercicio y la vestimenta.
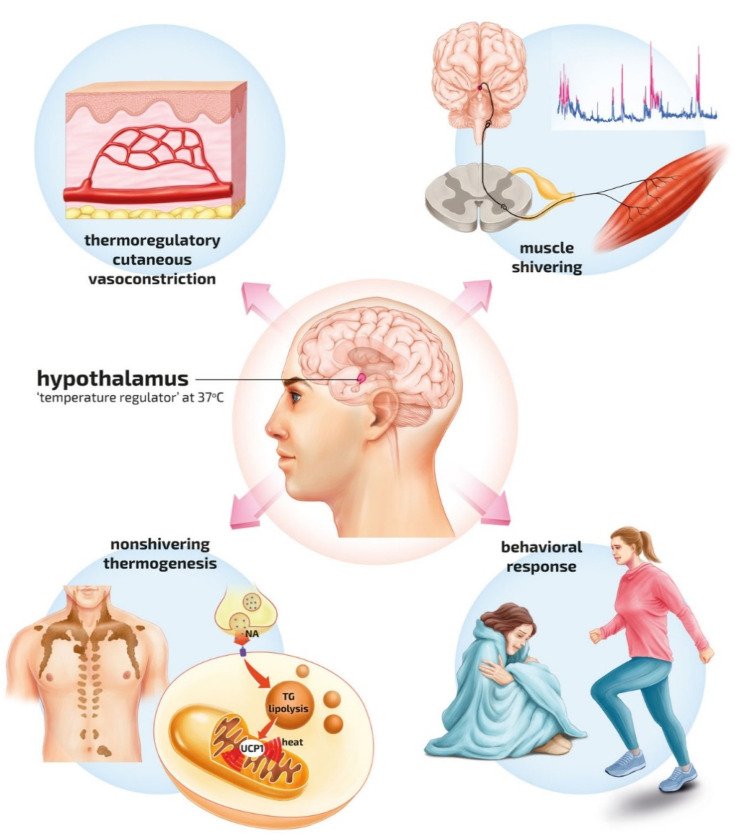
Vías fisiológicas de la termorregulación central y periférica contra el frío ambiental. El aumento del tono simpático causa vasoconstricción cutánea, lo que reduce el flujo sanguíneo de la piel y disminuye la pérdida de calor. La vasoconstricción aumenta el aislamiento del tejido, lo que reduce la transferencia de calor conductivo y minimiza la exposición de la sangre caliente al ambiente frío (arriba a la izquierda). La termogénesis por escalofríos en los músculos esqueléticos proporciona producción endógena de calor.
La contribución de los escalofríos a la producción de calor depende de la fuerza del estímulo frío. Cuanto más fuerte sea el estímulo, más intensa será la producción de calor. La intensidad de los escalofríos también depende del patrón dominante de escalofríos, escalofríos continuos o en ráfagas, y de la disponibilidad de sustratos energéticos, principalmente glucosa. Los escalofríos involuntarios pueden contrarrestar el enfriamiento al aumentar la producción de calor basal endógeno hasta un 500% del valor inicial (arriba a la derecha).
La termogénesis sin escalofríos ocurre en el tejido adiposo marrón.
La fuente de la termogénesis sin escalofríos es principalmente el desacoplamiento de la fosforilación oxidativa. Esto se logra mediante una fuga de protones mitocondriales a través de la proteína desacopladora 1 (UCP1) en el humano no aclimatado y un aumento en la termogénesis del tejido adiposo marrón después de la aclimatación al frío.
La UCP1 crea una fuga de protones a través de la membrana mitocondrial interna, desviando protones de la síntesis de ATP y dando como resultado la producción de calor (abajo a la izquierda). Las respuestas conductuales son actos motores somáticos dirigidos principalmente a minimizar la pérdida de calor o generar calor endógeno. La termogénesis inducida por el ejercicio proporciona la mayor ganancia de calor, alcanzando valores hasta 15-20 veces superiores a la tasa metabólica en reposo. El ejercicio en condiciones de frío puede no ser aconsejable, ya que conlleva un riesgo de sobreesfuerzo que conduce a un mayor enfriamiento y colapso circulatorio (abajo a la derecha).
En un individuo sano, la hipotermia puede ser el resultado de una transferencia excesiva de energía a un ambiente frío a través de conducción, convección, evaporación o radiación (hipotermia primaria). La hipotermia también puede ser causada por condiciones que deterioran la termogénesis o la termorregulación (hipotermia secundaria, Tabla 1 ).
Los niños y los adultos pequeños con índices de masa corporal (IMC) bajos son más susceptibles a la hipotermia debido a sus grandes proporciones de superficie corporal a peso, lo que permite una mayor pérdida de calor en comparación con individuos más grandes con IMC normales o altos. La hipotermia leve o moderada puede ocurrir en áreas urbanas y rurales en climas fríos y moderados durante todas las estaciones.
Los desastres naturales pueden poner a un gran número de víctimas en riesgo de hipotermia accidental.
La hipotermia severa es común en climas templados o fríos, así como en áreas montañosas. Los factores predisponentes incluyen ambientes fríos y húmedos, fatiga, agotamiento y gran altitud, con hipoxia. En un estudio de áreas montañosas, el 57% de las víctimas con lesiones graves (puntaje de gravedad de la lesión—ISS ≥ 16) y más de un tercio de las víctimas con lesiones graves con lesión cerebral traumática estaban hipotérmicas al ingreso hospitalario.
En otro estudio, más del 90% de los pacientes con trauma atrapados en vehículos de motor estaban hipotérmicos. Especialmente en pacientes con trauma, la hipotermia puede causar un aumento sustancial en la mortalidad y complicaciones por disminución de la contractilidad cardíaca, disritmias, coagulopatía inducida por trauma con mayor riesgo de sangrado y disminución de la respuesta inflamatoria.
Un estudio retrospectivo de registro de trauma europeo encontró que el 56% de los pacientes de al menos 16 años de edad, para quienes se disponía de datos de temperatura, con un puntaje de gravedad de la lesión (ISS) ≥ 9 y una temperatura central por debajo de 33 °C, vistos en el departamento de emergencias que murieron o fueron ingresados en una unidad de cuidados intensivos tenían falla multiorgánica.
La mortalidad general de este grupo fue del 32%. Se excluyeron los pacientes trasladados directamente a la UCI y no atendidos en urgencias, así como los pacientes con traumatismo craneoencefálico aislado. Dado que la hipotermia es más frecuente en pacientes con lesiones graves, es difícil determinar si existe una relación causal entre la hipotermia y el aumento de la mortalidad.
En Japón, la hipotermia es un problema común en espacios interiores para personas mayores con múltiples comorbilidades que viven solas, especialmente como complicación de lesiones, enfermedades o uso de medicamentos.
En muchos países, la hipotermia afecta y a menudo mata a los miembros más desfavorecidos de la sociedad, como las personas sin hogar y las personas adictas al alcohol o las drogas.
La hipotermia causa una disminución de los signos vitales y puede provocar un paro cardíaco ( Tabla 2 ). Un ambiente ventoso y húmedo acelera el enfriamiento. El índice de sensación térmica describe el efecto combinado de la temperatura ambiente y la velocidad del viento sobre la temperatura superficial de la piel.
En avalanchas, la velocidad de enfriamiento de las víctimas sepultadas puede alcanzar los 9 °C/h. La velocidad de enfriamiento de pacientes hipertérmicos durante la inmersión en agua a 1-2 °C puede alcanzar los 5 °C/10 min. La velocidad de enfriamiento de pacientes normotérmicos o hipotérmicos en agua fría depende en gran medida de las condiciones. Es mucho más lenta, pero aún significativa.
| Escenario | Hallazgos clínicos | Temperatura central estimada (°C) |
|---|---|---|
| Hipotermia I (leve) | Consciente, temblando* | 35–32 °C |
| Hipotermia II (moderada) | Alteración de la conciencia*; puede temblar o no. | <32–28 °C |
| Hipotermia III (grave) | Inconsciente*; signos vitales presentes | <28 °C |
| Hipotermia IV (grave) | Muerte aparente; signos vitales ausentes | Clásicamente < 24 °C ** |
* Los escalofríos o la consciencia pueden verse afectados por comorbilidades como traumatismos, afecciones del sistema nervioso central, toxinas o fármacos, como sedantes-hipnóticos u opioides, independientemente de la temperatura central.
** El paro cardíaco puede ocurrir en etapas tempranas o tardías de la hipotermia. Algunos pacientes pueden presentar constantes vitales con temperaturas centrales < 24 °C.
Una persona sumergida en agua fría (<15 °C) puede detenerse después de 30 min.
Después de la extricación de un entorno frío, el enfriamiento continúa por redistribución del calor desde el núcleo cálido a la periferia fría principalmente por intercambio de calor a contracorriente en la circulación periférica, pero también por conducción de calor desde el núcleo a los tejidos superficiales más fríos.
Los escalofríos pueden disminuir o eliminarse en pacientes que están exhaustos, sedados o gravemente enfermos. Sin escalofríos, la temperatura central cae más rápidamente y es probable que el recalentamiento espontáneo sea imposible.
Otros factores que pueden contribuir al enfriamiento rápido son la sudoración, el deterioro de la conciencia, el uso de una sola capa delgada de ropa, la falta de cobertura de la cabeza y un hábito corporal delgado con grasa subcutánea limitada. Durante el enterramiento por avalancha, la ausencia de una bolsa de aire y el desarrollo de hipercapnia también pueden conducir a un enfriamiento rápido.
En adultos jóvenes y sanos, el paro cardíaco inducido por hipotermia puede ocurrir por debajo de los 30 °C. En pacientes de edad avanzada y con comorbilidades, el miocardio puede volverse más irritable y el paro cardíaco inducido por hipotermia puede desencadenarse por debajo de los 32 °C.
Los signos vitales pueden permanecer presentes en pacientes con temperaturas centrales inferiores a 24 °C. El paro cardíaco hipotérmico es fundamentalmente diferente del paro cardíaco normotérmico. El tratamiento y los resultados difieren sustancialmente.
El colapso cardiocirculatorio durante la extricación o transferencia de pacientes hipotérmicos se conoce como colapso de rescate. Esto puede manifestarse como un paro cardíaco presenciado.
El mecanismo subyacente no se entiende bien y puede ser multifactorial. En pacientes hipotérmicos, el colapso de rescate puede ser coincidente durante el rescate, pero es más probable que sea causado por hipovolemia, disritmias cardíacas desencadenadas por intervenciones, como la cateterización venosa central, cambios bioquímicos o, con mayor frecuencia, por estímulos mecánicos como el movimiento repentino.
En pacientes hipotérmicos, el paro cardíaco también puede ser causado por afterdrop (enfriamiento adicional, incluso después de que haya comenzado el recalentamiento). La principal causa de afterdrop es la reperfusión de partes frías del cuerpo durante el recalentamiento, pero la transferencia de calor conductivo entre las regiones corporales más frías y más calientes también puede desempeñar un papel.
En un estudio, la temperatura central media de los pacientes con paro cardíaco hipotérmico presenciado fue de 23,9 ± 2,7 °C. Solo el 2,4 % presentó una temperatura central superior a 28 °C. En pacientes con temperaturas centrales superiores a 30 °C no se observó ningún paro cardíaco atribuible únicamente a la hipotermia.
En general, un nivel normal de consciencia se correlaciona con un bajo riesgo de paro cardíaco hipotérmico. En general, el colapso por rescate parece duplicar el riesgo de muerte en pacientes con hipotermia grave.
Se deben evitar las intervenciones, como los movimientos bruscos del paciente o la realización de ejercicios, que se sabe que causan colapso por rescate.
Diagnóstico de la hipotermia
El diagnóstico extrahospitalario de hipotermia accidental puede ser un desafío. Lo más importante es que se debe considerar y descartar la hipotermia accidental en pacientes con antecedentes de exposición al frío o condiciones predisponentes ( Tabla 1 ), y si el tronco se siente frío al tacto.
Si no se dispone de la medición de la temperatura central, se puede realizar un diagnóstico clínico evaluando los signos vitales ( Tabla 2 ). Los signos vitales generalmente disminuyen linealmente a medida que disminuye la temperatura central.
El escalofrío no es un síntoma constante. Se puede suprimir por varias razones y no se debe utilizar para diagnosticar el grado de hipotermia. Sin embargo, si un paciente tiembla, la temperatura central es ≥30 °C. El uso del nivel de conciencia es la mejor manera de evaluar la hipotermia si no se puede medir la temperatura central.
Sin embargo, el nivel de conciencia puede verse influenciado por otros factores además de la temperatura central, como la intoxicación y el traumatismo. Se debe utilizar el Sistema Suizo Revisado si no se puede medir la temperatura central ( Tabla 3 ).
| Etapa 1 | Etapa 2 | Etapa 3 | Etapa 4 | |
|---|---|---|---|---|
| Hallazgos clínicos 1 | “Alerta” de AVPU | “Verbal” de AVPU | “Doloroso” o “Inconsciente” de AVPU Signos vitales presentes | “Inconsciente” de AVPU Y Sin signos vitales detectables 2 |
| Riesgo de paro cardíaco 3 | Bajo | Moderado | Alto | Paro cardíaco hipotérmico |
| Oxígeno según la práctica clínica habitual, (objetivo: SpO 2 > 94%) 4 | + | + | + | + |
| Carbohidratos | Té dulce caliente, barras dulces. | Glucosa IV/IO. 5 | Glucosa IV/IO. 5 | − |
| Movimiento activo | + | − 6 | − | − |
| Recalentamiento pasivo | + | + | + | + |
| Recalentamiento activo | (+) | + | + | + |
| Movilización cautelosa/transporte horizontal si es posible | − | + | + | − |
| almohadillas de desfibrilación | – | + | + | + |
| Intubación | – | – | Considerar | + |
| RCP | – | – | – | + |
| Desfibrilación | – | – | – | + 7 |
| Medicamentos (RCP) | – | – | – | + 8 |
| Hospital con ECLS 9 | – | – | + | + |
1 En el sistema suizo revisado, «Alerta» corresponde a una puntuación GCS de 15. «Verbal» corresponde a puntuaciones GCS de 9 a 14, incluyendo pacientes confundidos. «Doloroso» e «Inconsciente» corresponden a puntuaciones GCS < 9. Si bien el escalofrío no se utiliza como un signo que define la etapa en el sistema suizo revisado, su presencia generalmente significa que la temperatura es >30 °C, una temperatura a la cual es improbable que ocurra una CA hipotérmica en pacientes sanos.
2 Sin respiración, sin pulso carotídeo o femoral palpable, sin presión arterial medible. Verifique si hay signos de vida (pulso y, especialmente, respiración) durante hasta 1 min.
3 La transición de colores entre las etapas representa la superposición de pacientes dentro de los grupos. El riesgo estimado de paro cardíaco se basa en que la hipotermia accidental es la única causa de los hallazgos clínicos. Si otras afecciones deterioran la conciencia, como asfixia, intoxicación, edema cerebral a gran altitud o trauma, el sistema suizo revisado puede predecir falsamente un mayor riesgo de paro cardíaco debido a la hipotermia. Se debe tener precaución si un paciente permanece «alerta» o «verbal» mostrando signos de inestabilidad hemodinámica o respiratoria como bradicardia, bradipnea o hipotensión porque esto puede sugerir la transición a una etapa con un mayor riesgo de paro cardíaco.
4 Podría ser difícil de medir debido a la vasoconstricción periférica.
5 Se debe administrar glucosa para la hipoglucemia. Si no se dispone de pruebas de glucosa en el punto de atención, se puede administrar glucosa empíricamente a un paciente hipotérmico con estado mental alterado.
6 Se permite el movimiento activo si hay escalofríos distintivos y el paciente ya está de pie o deambulando.
7 Si la fibrilación ventricular persiste después de tres descargas y la temperatura es <30 °C, retrase los intentos adicionales de desfibrilación hasta que la temperatura sea >30 °C.
8 Suspenda la epinefrina (adrenalina) y la amiodarona si la temperatura es <30 °C; aumente el intervalo de administración a 6-10 min para la epinefrina si la temperatura es de 30-35 °C. Además de los pacientes en paro cardíaco, los pacientes con temperaturas centrales < 30 °C, presión arterial sistólica < 90 mm Hg o arritmias ventriculares deben ser transferidos directamente a un centro de soporte vital extracorpóreo (ECLS); se pueden considerar los medios (+).
El diagnóstico definitivo y la determinación del nivel de hipotermia solo pueden realizarse mediante la medición de la temperatura central. Dado que las partes externas del cuerpo se enfrían más rápidamente que el núcleo, la temperatura central debe medirse lo más cerca posible de los órganos vitales (cerebro y corazón).
El termómetro ideal sería mínimamente invasivo, fácil de usar, higiénico, independiente de las condiciones ambientales, que mida la temperatura central con alta precisión y tenga un tiempo de respuesta corto.
No existe ningún dispositivo de medición de temperatura que satisfaga todos estos requisitos. Todos los termómetros tienen variaciones espaciales y temporales en la medición. Solo unos pocos estudios han evaluado la medición de la temperatura central en la hipotermia grave en humanos y aún menos han evaluado la medición de la temperatura central en ambientes fríos.
La Tabla 4 muestra los métodos de medición de la temperatura central, con sus características y limitaciones. Las mediciones periféricas, como la temperatura cutánea, la denominada arteria temporal, la temperatura oral y axilar, y la temperatura timpánica infrarroja, se ven influenciadas por las condiciones ambientales y no son precisas en casos de hipotermia.
Una excepción es la medición de la temperatura epitimpánica mediante termistor, que utiliza un dispositivo diseñado para uso en exteriores con buen aislamiento, si el conducto auditivo externo está permeable.
| Tipo de medición | Características | Limitaciones | Adecuación para la medición de la temperatura central en casos de hipotermia | Factible en el hospital (IH) o fuera del hospital (OH) |
|---|---|---|---|---|
| Tocar la piel del torso torso | No se necesita equipoAlto valor predictivo negativo | Estimación aproximada, solamenteNo validado para uso en ambientes fríos. | (+) | (OH)/IH |
| Arteria temporal (infrarroja) | Medición rápida, no invasiva, cómoda, de bajo coste e higiénica. | Retraso importante en el enfriamiento y el recalentamientoFuertemente afectado por la temperatura ambiente, la posición y la actividad vasomotora.Baja precisión | – | Ninguno |
| (Frente) Piel (radiación infrarroja, termistor electrónico, tira de cristal líquido) | Medición rápida, no invasiva, cómoda, económica e higiénica. | Puede ser varios grados inferior a la temperatura central.Altamente influenciado por la temperatura ambiente | – | Ninguno |
| Termómetro de microondas temporal | Rápido, no invasivo, fácil de usar.Se correlaciona bien con la temperatura cerebral, incluso en hipotermia severa. | Aún experimental, pero prometedor | (+) | IH |
| Termómetro de flujo térmico cero en la frente. La temperatura del tejido profundo se mide en la piel mediante una sonda de temperatura aislada. | Medición rápida, no invasiva y cómodaBuena concordancia con la temperatura central en normotermia e hipotermia leve | La equilibración tarda varios minutos.Mala concordancia con la disminución de la temperatura central (no confiable por debajo de 34 °C)No ha sido probado en ambientes fríos. | – | IH |
| Axilar (dispositivo electrónico o termómetro de vidrio + ) | Medición rápida, no invasiva, higiénica y cómoda. | Fuertemente afectado por la temperatura ambiente y el posicionamiento.La lectura es más baja que en otros lugaresRetraso de tiempo significativo durante el enfriamiento o el recalentamientoBaja precisión | – | Ninguno |
| Timpánica (radiación infrarroja) | Medición rápida, no invasiva, higiénica y cómoda. | Inexacto en pacientes hipotérmicosInexacto en ambientes fríos y calientes, si está mal colocado, con otitis media (hiperemia e inflamación), si la membrana timpánica está bloqueada por cerumen o con agua o nieve en el conducto auditivo externo.Baja precisión | – | (Yo) |
| Epitimpánico (termistor electrónico) | Buena correlación con la temperatura de la sangre arterial, incluso en enfriamiento y recalentamiento rápidos.Confiable para pacientes no intubados en uso extrahospitalarioFuerte correlación con la temperatura cerebral en varios estudios | Requiere canal auditivo externo abierto, buen aislamiento y fijación.Inicialmente requiere unos minutos para estabilizarseNo ampliamente disponibleInfluenciado por la temperatura de la cabeza y el cuelloInexacto durante un paro cardíacoNo es tan precisa como la medición de la temperatura central de la vejiga o el recto durante el estado estable. | + | OH/IH |
| Oral (termistor electrónico o termómetro de vidrio + ) | Medición rápida, no invasiva, higiénica y cómoda. | Influenciado por la posición, respiración con la boca abierta.No es preciso en entornos fríos y calientes.Baja precisiónInfluenciado por la temperatura de la cabeza y del cuello uterino | – | IH |
| Nasofaríngeo (termistor electrónico) | Rápido, mínimamente invasivoCalcula la temperatura del cerebro si se coloca aproximadamente a 10–14 cm de profundidad. | Sólo en pacientes sedados o anestesiadosLecturas falsas durante el enfriamiento y recalentamiento porque no se asegura la adherencia al tejido adyacente | + | OH/IH |
| Temperatura gastrointestinal (sensor de temperatura por telemetría) | Mayor validez en comparación con la medición rectal | Respuesta más lenta a los cambios que la medición esofágicaExperimentalUbicación impredecible.No es práctico. Debe ingerirse de 4 a 8 horas antes de su uso. | – | Ninguno |
| Esofágico (termistor electrónico) | Tercio inferior del esófago (aprox. 40 cm de profundidad de inserción desde los incisivos)Buena correlación con la temperatura de la sangre arterial, especialmente en estado estable.Estándar para pacientes intubados extrahospitalarios | Valores inexactos durante la cirugía de tórax abierto con enfriamiento cardíacoLa inserción de la sonda puede provocar vómitos y aspiración, hemorragia nasal, arritmias cardíacas y paro cardíaco. Puede quedar mal colocada en la tráquea.Relativamente contraindicado en pacientes con vías respiratorias no protegidas. | + | OH/IH |
| Vejiga (termistor electrónico) | Estrecha correlación con la temperatura de la sangre arterial en estado estacionarioTemperatura central confiable para uso hospitalario, uso generalizadoSe puede utilizar en combinación con la monitorización de la producción de orina. | Retrasos durante el enfriamiento o recalentamiento, aunque menores que con la medición rectal)Influenciado por la producción de orina (la diuresis fría aumenta la producción de orina).Es razonable si se requiere sonda urinaria. Puede ser incómodo para el paciente. Se requiere precaución al colocarla de forma higiénica. | + | IH |
| Rectal (termistor electrónico o termómetro de vidrio + ) | Estrecha correlación con la temperatura de la sangre arterial en estado estacionario | Inexacto si se coloca en las heces.La sonda debe insertarse 15 cm más allá del recto.Tiempo de retraso significativo durante el enfriamiento y el recalentamiento.Puede resultar embarazoso para el paciente. No es higiénico.Posible perforación del recto | + | IH |
| Catéter de arteria pulmonar (termistor electrónico) | Mide directamente la temperatura de la sangre que sale del corazón. Define la temperatura central. | No disponible fuera del hospital ni en muchos hospitales.Muy invasivo, con potencial de complicaciones graves. | + | IH |
| Temperatura cerebral | Mide la temperatura del cerebro. | Buena correlación con la temperatura central Sólo es posible en entornos experimentales o durante la neurocirugía. En general, es difícil rastrear la temperatura cerebral con otros sitios de monitoreo. | + | IH |
+ Ya no se pueden comprar termómetros de mercurio ni otros líquidos. El calor es radiación infrarroja de 300 GHz a 1 THz. La radiación de microondas tiene una frecuencia de 1 GHz a 300 GHz; (+) significa que puede considerarse, «+» es razonable, «-» no es razonable.
Los termómetros centrales no vasculares, como los termómetros esofágicos, de vejiga urinaria, rectales y nasofaríngeos, se correlacionan bien con la medición del catéter de la arteria pulmonar, el método más preciso para medir la temperatura central, en el estado estable.
Durante los cambios rápidos de temperatura, las lecturas de los termómetros centrales no vasculares se retrasan con respecto a la temperatura central real porque están influenciadas por el tejido circundante y los contenidos corporales, como el aire, la orina y las heces, que tienen inercia térmica.
Los termómetros no vasculares son más confiables durante un estado estable térmico, pero las lecturas siguen siendo a menudo discordantes. Si el conocimiento preciso de la temperatura cerebral real es crítico, se debe medir la temperatura esofágica o epitimpánica.
Se están desarrollando nuevos métodos, como los termómetros de microondas y de flujo de calor cero, para la medición no invasiva de la temperatura. Sin embargo, aún son experimentales y no son adecuados para la medición de la temperatura central en hipotermia profunda (<28 °C) o en un entorno frío.
En la práctica, se puede realizar una estimación aproximada inicial extrahospitalaria de la temperatura central tocando el pecho del paciente y utilizando el sistema suizo revisado. Si se dispone de la medición de la temperatura central, es mejor realizarla utilizando una sonda epitimpánica basada en termistor en pacientes no intubados y utilizando una sonda esofágica en pacientes intubados.
La medición nasofaríngea profunda extrahospitalaria (10-14 cm) puede ser una alternativa en pacientes con alteración de la conciencia y sin una vía aérea segura si no se dispone de un dispositivo epitimpánico basado en termistor.
En el hospital, la temperatura de la vejiga urinaria es un método alternativo ampliamente utilizado. Los dispositivos epitimpánicos infrarrojos son adecuados para detectar hipotermia, pero no para controlar la temperatura central.
Tratamiento hipotermia accidental
Tratamiento extrahospitalario
La temperatura central puede disminuir durante la atención médica, con la exposición, la analgesia, la anestesia y la infusión de líquidos. Es fundamental prevenir o retardar una mayor pérdida de calor y comenzar el recalentamiento lo antes posible.
Prevención de una mayor pérdida de calor
Se debe mantener la normotermia, pero el recalentamiento prehospitalario no es factible en la mayoría de los sistemas médicos de emergencia debido al equipo limitado y los cortos tiempos de transporte (<1 h). El énfasis debe estar en prevenir una mayor pérdida de calor.
Las medidas esenciales para los pacientes hipotérmicos en el entorno prehospitalario son la extracción del entorno frío, la limitación de una mayor pérdida de calor y el traslado rápido al hospital.
Los pacientes con mecanismos termorreguladores deteriorados y capacidad disminuida para tiritar debido a afecciones como traumatismos, hipotermia secundaria, uso de sedantes o bloqueo neuromuscular, tienen un alto riesgo de desarrollar hipotermia grave y paro cardíaco hipotérmico.
La prevención de la hipotermia es esencial para evitar complicaciones de la hipotermia y una mayor mortalidad. Los principios del manejo prehospitalario de la hipotermia dependen del estadio clínico ( Tabla 2 y Tabla 3 ).
Hipotermia leve (Etapa 1)
Los pacientes ilesos con hipotermia leve suelen estar completamente alertas. Generalmente, pueden ser atendidos en el lugar sin necesidad de traslado al hospital.
El recalentamiento pasivo, mediante la retirada del paciente del ambiente frío, la optimización del aislamiento, la oferta de alimentos y bebidas calientes y la promoción de movimientos activos, suele ser suficiente.
Hipotermia moderada o grave (Etapa 2 o 3)
Los pacientes con hipotermia moderada o grave requieren recalentamiento activo. Se debe aislar todo el cuerpo para reducir el riesgo de un mayor enfriamiento ( Figura 2 ).
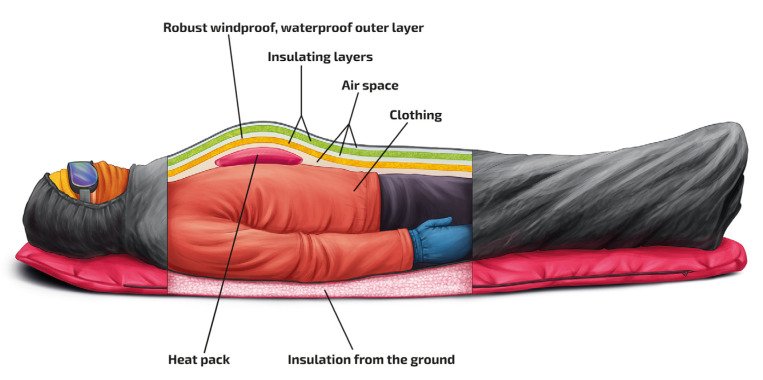
Se debe proporcionar protección contra el frío, el viento y la humedad. Un paciente hipotérmico debe ser abrigado con varias capas. Un paciente que no puede caminar debe ser colocado en posición horizontal en una camilla. Si hay ropa seca o capas disponibles, la ropa mojada debe cortarse en un entorno protegido.
Se deben aplicar grandes paquetes de calor químico o eléctrico al tronco en el pecho y la espalda, pero no deben tocar la piel, para prevenir quemaduras. Se debe agregar una barrera de vapor en condiciones de humedad o viento o si la ropa mojada no se puede quitar. Se deben colocar mantas o ropa seca dentro de la barrera de vapor.
Un paciente con ropa mojada que puede caminar debe cambiarse a ropa seca. Caminar aumenta la producción de calor, pero aumenta la caída posterior. A los pacientes hipotérmicos que se encuentran en posición horizontal no se les debe permitir caminar hasta que hayan consumido calorías y se les haya permitido tiritar durante aproximadamente 30 minutos.
El recalentamiento fuera del hospital puede ser difícil. Los intentos de recalentamiento no deben retrasar el transporte. Los pacientes hipotérmicos corren el riesgo de sufrir un paro cardíaco (PC).
Deben recibir una oxigenación adecuada y estar conectados a un monitor cardíaco. Se deben aplicar parches de desfibrilación en lugar de cables de monitorización, ya que reducen los artefactos electrocardiográficos por temblores, lo que permite una rápida detección y tratamiento de ritmos desfibrilables.
Si bien el acceso venoso periférico es deseable, puede ser difícil de obtener debido a la vasoconstricción periférica inducida por la hipotermia. Si no se puede establecer un acceso intravenoso (IV), se debe utilizar el abordaje intraóseo (IO).
Cuando se requieren líquidos intravenosos o intraóseos, estos se deben calentar a 38–42 °C y se deben administrar en bolos guiados por los signos vitales . El uso de fluidos calientes ayuda a limitar el enfriamiento secundario y puede proteger las líneas del congelamiento, pero tiene poco efecto directo sobre el recalentamiento.
En la hipotermia moderada o grave, la bradicardia y la presión arterial baja no requieren un tratamiento específico aparte del recalentamiento, ya que son respuestas a la disminución global del metabolismo celular.
Las arritmias supraventriculares, incluida la fibrilación auricular, suelen resolverse espontáneamente con el recalentamiento. La intubación endotraqueal es difícil en condiciones de frío. Las vías intravenosas pueden congelarse. La mayoría de los fármacos son ineficaces en la hipotermia. Los tubos endotraqueales se vuelven menos flexibles. La intubación endotraqueal generalmente debe posponerse hasta que el paciente esté en un entorno cálido.
Una vez en un entorno cálido, se debe utilizar la intubación endotraqueal de secuencia rápida. El riesgo de causar una arritmia maligna es mínimo en comparación con las ventajas de la oxigenación óptima y la protección de las vías respiratorias.
La rigidez y el trismo en pacientes con hipotermia grave pueden dificultar la intubación. El dióxido de carbono al final de la espiración (ETCO₂) no es fiable en casos de hipotermia grave.
Los pacientes deben ser ventilados utilizando parámetros estándar basados en el peso, sin depender del ETCO₂. La hiperventilación es menos perjudicial que la hipoventilación. Los pacientes deben ser transportados con suavidad y en posición horizontal para evitar un colapso por hipotermia (CA).
Hipotermia sin signos vitales (HT-IV)
Diagnóstico de paro cardíaco
Puede ser difícil diagnosticar una AC en un paciente inconsciente en un entorno frío. Los signos vitales pueden ser mínimos y extremadamente difíciles de detectar. Los reanimadores deben intentar detectar los signos vitales durante 60 s.
El uso de electrocardiografía, ETCO₂ (cualquier CO₂ espiratorio detectable se correlaciona con la presencia de signos vitales) o ecografía en el punto de atención (POCUS) puede ayudar a detectar la actividad cardíaca organizada y un gasto cardíaco significativo.
Reanimación cardiopulmonar (RCP)
Las compresiones torácicas y la ventilación de un paciente hipotérmico en CA deben realizarse como para un paciente normotérmico en CA. Si la fibrilación ventricular persiste después de tres descargas y la temperatura central es <30 °C, los intentos posteriores de desfibrilación deben retrasarse hasta que la temperatura central sea >30 °C.
No se debe administrar epinefrina ni amiodarona si la temperatura central es <30 °C. El intervalo de administración de epinefrina debe duplicarse de cada 3-5 minutos a cada 6-10 minutos si la temperatura central es <30 °C. Los protocolos estándar deben reanudarse una vez que se alcance la normotermia (≥35 °C).
Triage prehospitalario
En un paciente hipotérmico con PC, no se debe iniciar la RCP o se debe finalizar si hay una orden válida de «no resucitar», signos claros de muerte irreversible, incluyendo lividez dependiente fija (livor mortis), peligro o agotamiento de los rescatadores, o sepultura por avalancha de más de 60 min con asistolia y vía aérea completamente obstruida.
En un paciente hipotérmico, la rigidez (rigor mortis aparente) no es un signo fiable de muerte.
Las siguientes condiciones no son contraindicaciones para el recalentamiento de un paciente hipotérmico en PC: asistolia, PC no presenciada, temperatura central baja, tiempo prolongado sin flujo o con flujo bajo, pupilas fijas y dilatadas, hipocapnia (ETCO2 <10 mmHg), edad avanzada o traumatismo (incluso traumatismo mayor).
Derivación y transporte de pacientes

Los criterios para la transferencia directa de un paciente hipotérmico a un centro ECLS son paro cardíaco, temperatura central < 30 °C, presión arterial sistólica < 90 mmHg o disritmia ventricular. Dependiendo del entorno y la distancia desde un centro ECLS, se puede utilizar una parada en un hospital que no sea ECLS para realizar un triage hospitalario, como la puntuación de estimación de probabilidades de supervivencia HOPE.
Se debe utilizar RCP mecánica para rescates y transportes prolongados o técnicamente difíciles. Si el transporte con RCP continua no es posible, una alternativa es realizar RCP intermitente ( Figura 3 ).
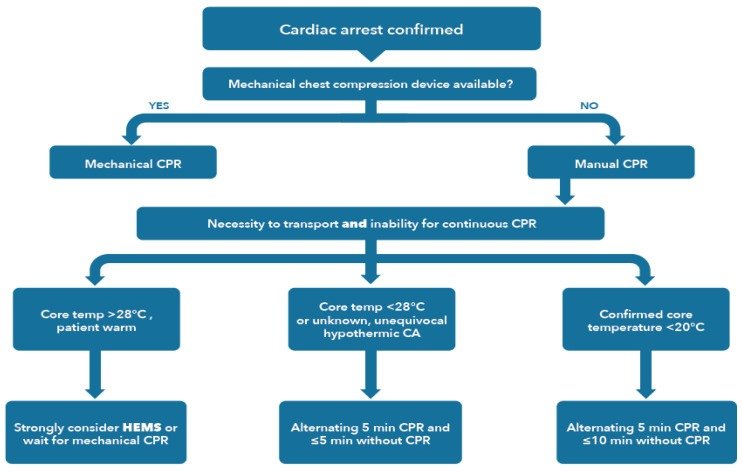
Algoritmo de RCP intermitente para pacientes con hipotermia grave (<28 °C) en paro cardíaco cuando no son posibles las compresiones torácicas continuas. CORRECCIONES CRÍTICAS: 1. La frase «paciente caliente» no significa que el paciente esté caliente.
Significa que el paciente no está lo suficientemente hipotérmico para la RCP intermitente. 2. «Alternando 5 min de RCP» y ≤5 min o ≤10 min sin RCP debe decir: «Alternando al menos 5 min de RCP y ≤5 min o ≤10 min sin RCP». Copyright 2021 Elsevier y European Resuscitation Council
Cuando no sea posible realizar compresiones torácicas continuas en un paciente con una temperatura central < 28 °C o si se desconoce dicha temperatura, pero las circunstancias son inequívocas para un paro cardíaco inducido por hipotermia, alterne al menos 5 min de RCP con ≤ 5 min sin RCP. En pacientes con una temperatura < 20 °C, alterne al menos 5 min de RCP con ≤ 10 min sin RCP.
Una vez que un paciente sufre un paro cardíaco hipotérmico, ya no es necesario evitar los movimientos rápidos. Si bien es razonable transportar a un paciente con RCP en curso en posición horizontal, no hay suficientes datos disponibles para emitir recomendaciones definitivas.
El transporte rápido, incluso en una posición no horizontal, es preferible al transporte lento en posición horizontal.
Tratamiento hospitalario
Las opciones de tratamiento hospitalario dependen del estado circulatorio, la etapa de hipotermia y los recursos disponibles ( Figura 4 ).
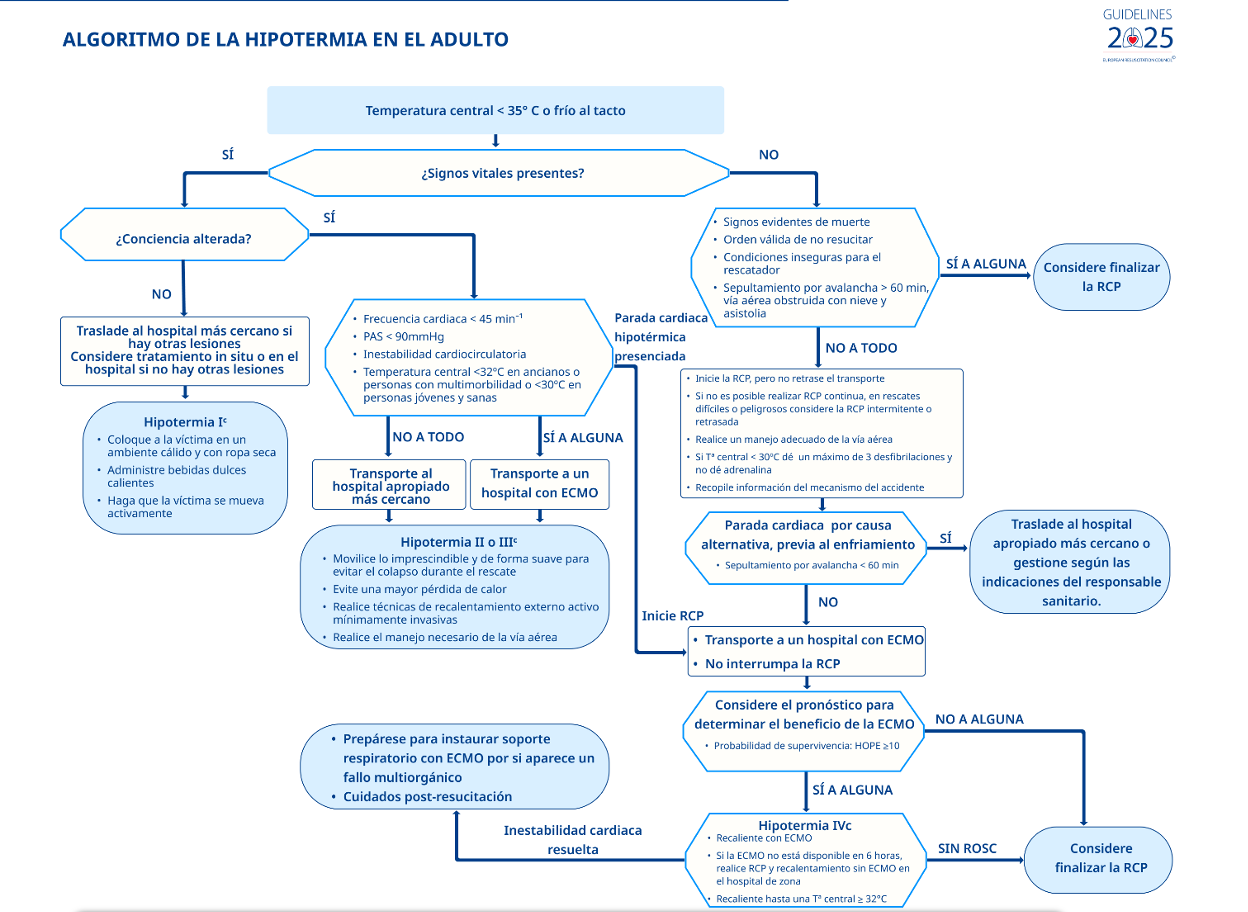
Video resumen hipotermia accidental
Los pacientes con circulación estable deben recalentarse con técnicas de recalentamiento externo pasivo y activo ( Tabla 5 ). En pacientes con riesgo de paro cardíaco o con circulación inestable, el ECLS debe mantenerse en espera e iniciarse rápidamente si es necesario.
Los pacientes con PC hipotérmica o inestabilidad hemodinámica requieren soporte cardiocirculatorio además del recalentamiento interno activo. Esto se logra mejor con el ECLS ( Tabla 5 ).
| Técnica de recalentamiento | Frecuencia de recalentamiento | Notas y controversias | Complicaciones del recalentamiento |
|---|---|---|---|
| Recalentamiento pasivo | |||
| Recalentamiento pasivo | 0,5–4 °C/h (depende de la función termorreguladora y de las reservas metabólicas del paciente) | Protege contra una mayor pérdida de calor y permite que el paciente se caliente por sí solo. | Insignificante en hipotermia leve aislada. En pacientes con frío intenso y con hipotermia secundaria o comorbilidades, el recalentamiento pasivo por sí solo no es suficiente. |
| Recalentamiento pasivo con movimiento activo | 1–5 °C/h | Hacer ejercicio inmediatamente después del rescate aumenta la postcaída | Un aumento de la postcaída podría causar un colapso del rescate |
| Recalentamiento externo activo | |||
| Recalentamiento activo que incluye recalentamiento de superficies con aire forzado, almohadillas térmicas, por ejemplo, Arctic Sun®, líquidos intravenosos calentados (40 °C). | 0,5–4 °C/h | Protege de una mayor pérdida de calor, proporciona calor externo. Los líquidos intravenosos calentados no son eficaces si se utilizan como único método de recalentamiento | Similar al recalentamiento pasivo |
| Recalentamiento interno activo | |||
| Lavado de vejiga | Variable. Añade < 0,5 °C/h | No recomendado. El recalentamiento es intermitente y lento debido a la pequeña superficie. Control deficiente de la temperatura de la infusión. | Insignificante a menos que el cateterismo sea difícil |
| Lavado gástrico | Puede añadir ~0,5–1 °C/h | No recomendado. Relación riesgo-beneficio inaceptablemente alta. | Posibilidad de aspiración, cambios de líquidos y electrolitos. |
| Recalentamiento de catéteres intravasculares, p. ej., CoolGuard ® Quattro ® Cool Line ® Innercool ® | Específico del dispositivo (añade ~0,5–2,5 °C/h) | Indicaciones de uso inciertas. Posible beneficio para pacientes con resfriados, especialmente aquellos con comorbilidades, con circulación estable. | Posibilidad de hemorragia o trombosis, que puede empeorar la hipotensión arterial en pacientes inestables. |
| Lavado torácico o peritoneal | Variable, dependiendo de la temperatura y del caudal de irrigación paricardial. | Puede ser útil en pacientes inestables cuando no se dispone de recalentamiento ECLS. Es muy invasivo. | Posibilidad de hemorragia, traumatismo pulmonar o intestinal, y alteración de líquidos y electrolitos. El lavado torácico puede interferir con la RCP. |
| CRRT (incluyendo CVVHF, CVVHD, CVVHDF) | Añade ~1,5–3 °C/h | No se recomienda a menos que no se disponga de recalentamiento ECLS. Requiere presión arterial adecuada. Se requiere heparinización, anticoagulación con citrato o prostaciclina. | Problemas poco frecuentes. Complicaciones vasculares locales. Embolia gaseosa. Hipotensión arterial. |
| Hemodiálisis | Añade ~2–3 °C/h | El paciente debe ser capaz de aumentar el gasto cardíaco para perfundir el circuito externo. Se requiere heparinización. | Posibilidad de hipotensión arterial, hemorragia, trombosis, hemólisis, etc. |
| Recalentamiento veno-venoso (generalmente con ECMO) | ~4–10 °C/h | No proporciona soporte circulatorio ni ventilatorio en caso de paro cardíaco. El paciente debe ser capaz de aumentar el gasto cardíaco para perfundir el circuito externo | Posibilidad de hipotensión arterial, hemorragia, trombosis, hemólisis, etc. |
| Soporte vital extracorpóreo (ECLS; VA-ECMO, CPB incluyendo circulación extracorpórea mínimamente invasiva (MiECC) | ~4–10 °C/h | Método de recalentamiento preferido para pacientes en paro cardíaco. Se prefiere la ECMO a la CEC. La ECMO puede utilizarse por vía femoral, evitando la necesidad de esternotomía. Puede utilizarse para tratar complicaciones pulmonares posteriores al recalentamiento, como el SDRA. | Posibilidad de hemorragia e hipotensión arterial, trombosis, hemólisis, etc., como ocurre con todos los dispositivos intravasculares. |
- CPB: bypass cardiopulmonar.
- RCP: reanimación cardiopulmonar.
- ECLS: soporte vital extracorpóreo.
- ECMO: oxigenación por membrana extracorpórea.
- TRRC: terapia de reemplazo renal continuo.
- CVVHF: hemofiltración venovenosa continua.
- CVVHD: hemodiálisis venovenosa continua.
- CVVHDF: hemodiálisis venovenosa continua con filtración.
En pacientes con circulación espontánea y una temperatura central de 33-36 °C, el objetivo del recalentamiento debe ser la normotermia, con una temperatura central de aproximadamente 37 °C. En pacientes con paro cardíaco hipotérmico, la prioridad principal es el retorno a la circulación espontánea (RCE), ya que la perfusión orgánica fisiológica mejora el aporte de oxígeno y reduce el daño orgánico por falta de flujo y bajo flujo durante la PC, en comparación con la RCP. Una vez establecido el RCE, el objetivo debe ser el control de la temperatura según los protocolos locales.
El recalentamiento es pasivo si el paciente aumenta su temperatura central sin calor exógeno, y activo si se administra calor exógeno. El recalentamiento activo puede ser externo o interno, según el método de transferencia de calor ( Tabla 5 ). La mayoría de los pacientes requieren recalentamiento externo pasivo y activo. Los pacientes en paro cardíaco y aquellos que no pueden recalentarse con recalentamiento externo activo requieren recalentamiento interno activo ( Tabla 5 ).
En caso de hipotermia leve (HTA), se debe recalentar a los pacientes mediante recalentamiento externo pasivo y activo, y mediante recalentamiento interno mínimamente invasivo con líquidos calientes por vía oral ( Figura 4 ). El escalofrío y el movimiento activo acelerarán aún más el recalentamiento. Se debe permitir el escalofrío si no existen contraindicaciones, como dolor por lesiones o riesgo de lesión miocárdica causado por un mayor consumo de oxígeno en un paciente con alto riesgo cardiovascular.
En pacientes con hipotermia moderada o grave (HT II o HT III), es necesario el recalentamiento activo. Por lo general, el recalentamiento externo activo es eficaz. Si un paciente no se recalienta adecuadamente, se debe utilizar el recalentamiento interno activo. Los signos de falla del recalentamiento incluyen temperatura central que permanece igual o disminuye, aumento de los niveles de lactato, disminución del nivel de consciencia, disminución de la presión arterial o la aparición de arritmias ventriculares.
Los métodos de recalentamiento interno activo en la hipotermia moderada a grave incluyen catéteres de recalentamiento intravascular y terapia de reemplazo renal continuo (TRRC, Tabla 5 ). Las complicaciones, como sangrado, trombosis venosa profunda e infección, son más comunes que con el recalentamiento externo activo.
Los pacientes sin signos vitales (HT IV) están en paro cardíaco y requieren soporte cardiocirculatorio. El método preferido es el recalentamiento con soporte vital extracorpóreo (ECLS). Se desconoce la velocidad ideal de recalentamiento. La velocidad objetivo de recalentamiento debe ser ≤5 °C/h.
Una velocidad más lenta de recalentamiento (aproximadamente 2 °C/h) puede estar asociada con una mejor supervivencia con un buen resultado neurológico. Se prefiere la oxigenación por membrana extracorpórea (ECMO) a la derivación cardiopulmonar (CPB), porque la ECMO se puede mantener después de la RCE y se puede utilizar para mantener el soporte vital mientras se resuelve el síndrome de dificultad respiratoria del adulto (SDRA), una secuela común de la hipotermia.
El recalentamiento sin ECLS solo se debe considerar cuando el recalentamiento con ECLS no está disponible y no se puede proporcionar dentro de las 6 h. No se ha determinado el paquete ideal de recalentamiento sin ECLS. El recalentamiento debe emplear técnicas disponibles localmente y conocidas por el personal médico, como mantas térmicas, recalentamiento con aire forzado externo y lavado peritoneal.
Si bien los líquidos intravenosos no son eficaces para el recalentamiento, deben calentarse a 40 °C para evitar el enfriamiento. La RCP debe mantenerse de forma continua hasta alcanzar la recuperación de la circulación espontánea (RCE). La compresión torácica mecánica puede ser útil en la RCP de larga duración. El equipo debe estar capacitado para evitar tiempos prolongados sin intervención y para prevenir lesiones al paciente.
En la hipotermia moderada y grave, el volumen sanguíneo circulante disminuye debido a una combinación de desplazamiento del plasma extravascular y una ingesta insuficiente de líquidos. En pacientes expuestos al frío durante varias horas, la diuresis inducida por el frío puede reducir aún más el volumen intravascular. Los pacientes sumergidos durante horas pueden presentar diuresis inducida por presión hidrostática y una depleción hídrica grave [ 76 ]. Al mismo tiempo, la centralización circulatoria puede reducir el espacio vascular. La reposición de volumen debe administrarse con precaución para evitar la sobrecarga. Idealmente, la reposición de volumen debe administrarse con monitorización de la presión venosa central.
Durante el recalentamiento, se elimina la vasoconstricción inducida por hipotermia que previamente limitaba el espacio vascular. Se debe reemplazar el volumen para evitar una depleción grave del volumen con el shock resultante. La interpretación de los gases en sangre se debe realizar de acuerdo con el enfoque alpha-stat, evaluando las muestras de gases en sangre a 37 °C. Esto conduce a una mejor perfusión cerebral y un mejor resultado neurológico en comparación con el uso de valores de gases en sangre arterial corregidos por la temperatura.
Algunos estudios sugieren que en pacientes con hipotermia grave, el gradiente PaCO2 – ETCO2 aumenta . Esto puede ayudar a confirmar un diagnóstico de hipotermia accidental en circunstancias poco claras.
Se han desarrollado varias herramientas para ayudar a predecir el resultado. La puntuación Hypothermia Outcome Prediction after Extracorporeal Life Support (HOPE) es actualmente la mejor herramienta de predicción disponible y se debe utilizar para evaluar si es probable que un paciente hipotérmico en paro cardíaco se beneficie del recalentamiento ECLS.
Las lesiones por congelación que aún están congeladas deben descongelarse tan pronto como la circulación y la temperatura central se hayan estabilizado.
Reanimación cardiopulmonar extracorpórea

La reanimación cardiopulmonar extracorpórea (RCPE) seguida de recalentamiento con ECLS puede estar asociada con una mayor supervivencia y resultados neurológicos más favorables que la RCP convencional sola en pacientes con hipotermia accidental sin signos vitales.
El rápido progreso tecnológico, incluida la miniaturización y la mejora de la eficacia, seguridad y transportabilidad de los dispositivos de ECLS, está ampliando las posibilidades de la RCPE y el recalentamiento con ECLS.
Es posible obtener buenos resultados neurológicos, incluso con tiempos prolongados sin flujo o con flujo bajo, pero solo si se desarrolló hipotermia antes del paro cardíaco. Debido a las bajas tasas de supervivencia y la alta probabilidad de morbilidad importante en pacientes no seleccionados, no se debe utilizar ECPR si la temperatura central es >30 °C, hay un traumatismo importante o hay comorbilidades que no son compatibles con una calidad de vida aceptable si el paciente se recupera. La ECPR, proporcionada en un centro con experiencia y protocolos optimizados, puede mejorar la supervivencia y los resultados neurológicos.
La ECMO venoarterial (VA) es el método preferido de ECPR porque los requisitos de anticoagulación son mínimos y porque la ECMO VA puede proporcionar soporte circulatorio y respiratorio más allá del ROSC.
Las probabilidades de supervivencia son mayores después del recalentamiento con ECMO que con CPB. Las probabilidades de supervivencia también son mayores en pacientes con paros cardíacos hipotérmicos presenciados que en aquellos con AC hipotérmicos no presenciados. Las víctimas de avalanchas tienen la menor probabilidad de sobrevivir. El sexo masculino, la temperatura corporal inicial alta, el pH bajo y el potasio sérico alto se asociaron con menores probabilidades de supervivencia.
Se han descrito enfoques prácticos para el manejo de pacientes con recalentamiento mediante ECPR y ECLS. Por lo general, se necesitan medidas adicionales, como la reanimación vigorosa con líquidos isotónicos y el uso de vasopresores, para mantener la presión arterial media entre 50 y 70 mmHg. Las alteraciones graves del equilibrio ácido-base y de la coagulación, así como otros problemas, pueden requerir tratamiento adicional. La temperatura central debe monitorizarse cuidadosamente ( Tabla 4 ).
Los pacientes en paro cardíaco hipotérmico deben recibir ECPR continua hasta que se logre ROSC. Puede justificarse apoyo adicional con ECLS después de ECPR. Sin embargo, la decisión de continuar la atención sin signos de mejoría significativa inmediata es difícil.
Los predictores de supervivencia se han descrito en estudios retrospectivos. El lactato sérico inicial más bajo, el pH más alto y la edad más joven se asociaron con mejores resultados neurológicos en los sobrevivientes de OHCA hipotérmico tratados con ECPR.
Actualmente no hay un predictor simple y confiable de la eficacia o el resultado de ECPR. El manejo de temperatura objetivo (TTM) se debe realizar de acuerdo con los protocolos locales. Se debe evitar la hipertermia posterior a la reanimación. Se desconoce el momento de ECPR y la temperatura objetivo óptima después de ECPR.
Se debe considerar la interrupción de la ECPR si no se alcanza la RCE a la temperatura central objetivo. La decisión de suspender el tratamiento también puede basarse en factores clínicos adicionales, como la aparición de una hemorragia incontrolable, información adicional sobre la causa de la AC o signos de lesión cerebral anóxica grave. La muerte cerebral es una causa frecuente de muerte tras la ECPR. Se debe considerar la donación de órganos.
Pronostico del paciente con hipotermia
En comparación con otras afecciones que pueden provocar un paro cardíaco, la hipotermia accidental es poco frecuente. Incluso los centros grandes rara vez tratan a más de 20 pacientes al año. Los estudios más amplios hasta la fecha han incluido solo unos pocos cientos de pacientes.
La agrupación de datos es importante para acelerar el desarrollo de métodos de diagnóstico, tratamiento y predicción de resultados. El Registro Internacional de Hipotermia ya ha recopilado datos de más de 200 pacientes. Se necesitan más contribuciones y son bienvenidas.
Un paciente con hipotermia leve que se encuentra en posición horizontal debe descansar y se le debe permitir temblar antes de permitirle ponerse de pie o caminar, pero algunas pautas sugieren que, si el paciente puede moverse con seguridad, el esfuerzo físico inmediato acelera el recalentamiento y facilita la evacuación terrestre en terrenos difíciles.
La puntuación HOPE intrahospitalaria ha mejorado sustancialmente la predicción de resultados para pacientes hipotérmicos en paro cardíaco que son tratados con recalentamiento ECLS. Una puntuación HOPE prehospitalaria podría facilitar las decisiones de tratamiento y transporte en el campo.
Cuando no se dispone de recalentamiento ECLS, se deben utilizar medidas que no sean ECLS. Actualmente no existen datos sobre la eficacia y seguridad de varias medidas que no sean ECLS. Se requieren con urgencia estudios de alta calidad sobre recalentamiento que no sean ECLS en pacientes hipotérmicos en CA.
Conclusiones
La hipotermia accidental es una caída involuntaria de la temperatura central por debajo de 35 °C. Anualmente, miles mueren de hipotermia primaria y un número desconocido muere de hipotermia secundaria en todo el mundo. Se puede esperar hipotermia en pacientes de emergencia en la fase prehospitalaria. Los pacientes lesionados e intoxicados se enfrían rápidamente incluso en regiones subtropicales.
Las medidas preventivas son importantes para evitar la hipotermia o el enfriamiento en pacientes enfermos o lesionados. El diagnóstico y la evaluación del riesgo de paro cardíaco se basan en los signos clínicos y la medición de la temperatura central cuando esté disponible.
Los pacientes hipotérmicos con factores de riesgo de paro cardíaco inminente (temperatura < 30 °C en pacientes jóvenes y sanos y < 32 °C en personas mayores o pacientes con múltiples comorbilidades), arritmias ventriculares o presión arterial sistólica < 90 mmHg) y los pacientes hipotérmicos que ya están en paro cardíaco, deben ser transferidos directamente a un centro de soporte vital extracorpóreo (ECLS). Si un paciente hipotérmico sufre un paro cardíaco, se debe realizar reanimación cardiopulmonar (RCP) continua.
En pacientes hipotérmicos, las probabilidades de supervivencia y un buen pronóstico neurológico son mayores que en pacientes normotérmicos en caso de paro cardíaco presenciado, no presenciado y asistólico. Se deben utilizar dispositivos de RCP mecánica para un rescate prolongado, si están disponibles. En pacientes con hipotermia grave en paro cardíaco, si no es posible la RCP continua o mecánica, se debe utilizar la RCP intermitente.
El recalentamiento puede lograrse mediante técnicas pasivas y activas. Con mayor frecuencia, se utilizan técnicas externas pasivas y activas. Solo en pacientes con hipotermia refractaria o paro cardíaco se requieren técnicas de recalentamiento interno.
El recalentamiento ECLS debe realizarse con oxigenación por membrana extracorpórea (ECMO). Un paquete de cuidados posteriores a la reanimación debe complementar el tratamiento.
Infografía Hipotermia accidental
Autores
Peter Paal, Mathieu Pasquier , Tomasz Darocha, Raimund Lechner , Sylweriusz Kosinski , Bernd Wallner , Ken Zafren, Hermann Brugger.
Bibliografía
Int J Environ Res Salud Pública. 3 de enero de 2022;19(1):501.
doi: 10.3390/ijerph19010501
ID de producto: PMC8744717 ID de producto: 35010760









Deja un comentario